Можно ли из морской воды сделать питьевую?
30.09.2014Штиль. Бессильно обвисшие паруса испанского галеона. Солнечные лучи, дробящиеся на тысячи осколков. Океан расплавленного серебра, простирающийся до самого горизонта. Три недели абсолютной неподвижности. Изможденный матрос у штурвала, безнадежно смотрящий в чистое, без единого облачка, небо. Срок жизни двухсот человек, выживших после встречи с объединенным флотом Вольного Братства, исчисляется запасом теплой и затхлой воды, лениво плещущейся в просмоленных дубовых бочках.

Так могла бы начинаться очередная глава «Одиссеи капитана Блада» или рассказ из серии «Легенды Южных Морей». Жажда – бич потерпевших кораблекрушение, уносит жизни людей, иногда находящихся всего в полшаге от спасения. Страшная смерть от обезвоживания посреди безграничного водного пространства. Изощренное коварство мироздания.
Что же мешает использовать океанскую воду в качестве питьевой? Повышенное содержание соли и прочих минеральных веществ. Предельно допустимая норма – 1грамм растворимых солей на литр воды. Морская (океанская) вода, попав в организм человека, вызывает катастрофические нарушения состава крови и полную остановку почечной деятельности. Результат – быстрая, но мучительная смерть.
Неужели в наш просвещенный 21 век нет способа превратить соленую морскую воду в пресную питьевую? Есть и не один. Известны три основных, применимых за пределами научных лабораторий, метода опреснения воды. Рассмотрим каждый из них по подробнее.
Дистилляция или перегонка
Известный с I века нашей эры метод разделения растворов на жидкую фазу и сухой остаток. Применялся Авиценной для получения эфирных масел. Позволю себе напомнить читателю небольшой кусочек школьного курса физики, не для того, чтоб показаться умнее, а исключительно для более ясного понимания процесса. Плотность одного и того же вещества в жидкой и газообразной форме отличается в сотни раз. Следовательно, и способность удерживать в себе растворенные компоненты другого вещества подчиняется той же эмпирической пропорции. Туманно и неясно? Сейчас упрощу. Содержание морской соли в океанской воде – 20 грамм на литр. Плотность воды 1000 кг/м/куб., плотность пара при нормальном, 720 мм/ртутного столба, давлении – 1 кг/м/куб. Разница в 1000 раз. Проведя несложные вычисления, получаем следующий результат: при испарении 1 литра морской воды, содержащей 20 грамм соли, мы получим n-ый объем пара с содержанием соли 0,02 грамма. Теперь дело за малым, снова превратить пар в жидкость и наслаждаться идеальным вкусом дистиллированной воды. Практическое решение данной задачи выглядит следующим образом. Некоторый объем морской воды испаряют методом нагревания в замкнутом сосуде, а полученный пар отводят по трубке в другой сосуд, с более низкой температурой. Конденсат, оседающий на стенках холодильника – и есть опресненная морская вода.
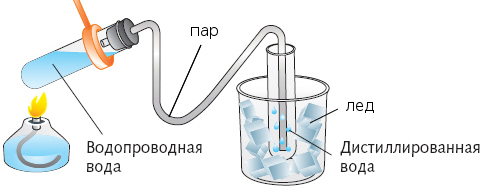
Кстати, на спасательных плотах используют дистилляторы воды, работающие по такому же принципу, только нагревательным элементом служит солнце. Благодаря черному покрытию резервуар с морской водой нагревается сильнее окружающей среды. Пар, осев на стенках пленки, охлаждается за счет более низкой температуры воздуха и, превратившись в капельки дистиллированной воды, стекает в специально отведенную емкость.

Опреснение методом ионного обмена
И снова вспоминаем школьный курс, на этот раз, химии. С точки зрения этой науки, морская вода представляет собой раствор электролита, содержащий в себе положительно и отрицательно заряженные ионы поваренной соли (NaCl), катионы и анионы. Воздействуя различными химическими способами на электролит, можно заставить ионы раствора, независимо от заряда, собраться в определенном месте и тем самым освободить от своего присутствия значительный объем жидкости. Практическое воплощение. Ионообменный опреснитель представляет собой замкнутый сосуд (электролитическую ванну), внутренний объем которой поделен на три части полупроницаемыми пластинами ионитов – сетчатых полимеров, изготовленных на основе гелевых материалов. Иониты заполнены жестко зафиксированными ионами различных металлов и различаются по знаку заряда. При подаче морской воды в опреснитель, отрицательно заряженные ионы собираются на положительно заряженной пластине ионита, положительно заряженные – на отрицательной. А между ними остается пространство, заполненное пресной, идеально чистой, водой.
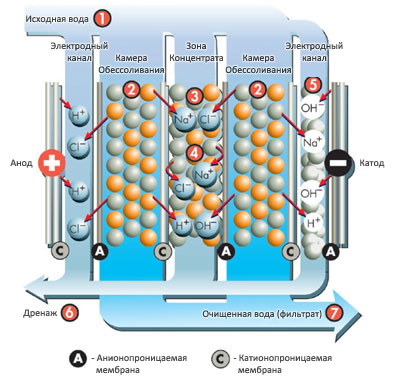
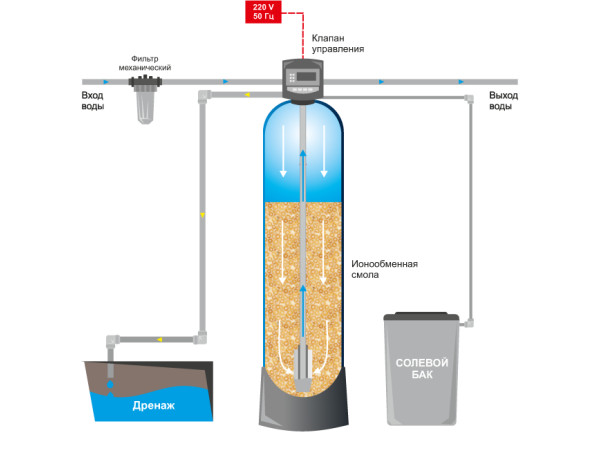
Преимущества ионообменного опреснения очевидны – для протекания реакции не требуется внешний источник энергии, регенерация выработавших свой ресурс пластин–ионитов проводится путем промывки их пресной водой. На том же принципе работают и бытовые фильтры умягчители, снижающие жесткость водопроводной воды.
Опреснители на основе явления обратного осмоса
Этот метод далеко не нов, он используется с начала 70-х годов прошлого столетия для обеспечения потребности в пресной воде океанских буровых платформ. Не углубляясь в дебри физических основ и определений осмотического давления жидкостей, кратко опишу сам процесс опреснения. Фильтр обратного осмоса – это, по сути, фильтрация жидкости (воды) сквозь полупроницаемую мембрану, размер пор которой лишь немногим больше размера молекулы фильтранта.
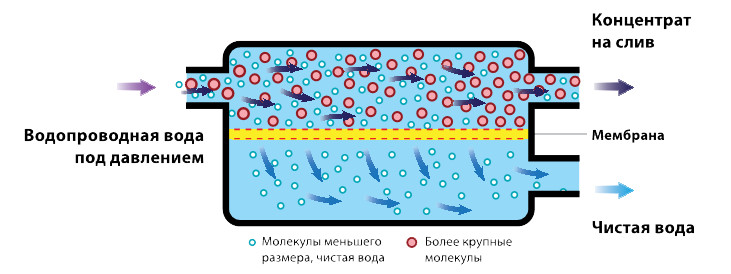
Через такое «сито» проходят только молекулы Н2О, а ионы соли и остальные, растворенные в морской воде минералы, остаются «запертыми» в замкнутом объеме бачка–отстойника. Метод, как и все гениальное, прост в реализации и требует соблюдения всего лишь одного условия – высокого давления фильтруемой жидкости. Так, в бытовых очистителях, работающих на явлении обратного осмоса, используются нагнетающие насосы с номиналом 3-5 атмосфер (если не достаточно давления в системе), на станциях опреснения морской воды – до 70 атмосфер. Также, домашние фильтры оснащены несколькими ступенями предварительной очистки воды, что позволяет существенно продлить срок службы основного и весьма недешевого элемента – осмотической мембраны.



